تعداد پیوندهای کربن در گرافیت
در بخش 5 شیمی سال دوم دبیرستان ، که به تازگی تغییراتی در آن ایجاد شده است ، می خوانیم : « در هر لایه از گرافیت ، هر اتم کربن با 4 پیوند و با آرایش سه ضلعی مسطح به سه اتم کربن دیگر متصل است » . آیا واقعاً هر اتم کربن 4 پیوند تشکیل داده است یا 3 پیوند ؟
اتم های کربن پیش از تشکیل پیوند ، می بایست برانگیخته شوند ، یعنی از آرایش 1s2 2s2 2p2 به آرایش 1s2 2s1 2p3 درآیند . سپس اوربیتال 2s با دو اوربیتال x , y از زیر لایه ی 2p هیبرید می شوند و سه اوربیتال sp2 تشکیل می دهند . حال این سه اوربیتال تک الکترونی از هر اتم در تشکیل سه پیوند یگانه σ ( سیگما ) با آرایش سه ضلعی مسطح شرکت می کنند . اما تکلیف تک الکترون باقیمانده در اوربیتال هیبرید نشده ی 2pz چه می شود ؟ آیا این اوربیتال در تشکیل پیوند شرکت نمی کند ؟ منابع علمی می نویسند که این الکترون نامستقر است . آیا این جمله بدین معنی است که این الکترون در همان اوربیتال اولیه اش باقی می ماند و در موقع لزوم از آن فرار می کند ؟ نامستقر بودن الکترون چهارمِ هر اتم کربن ، به معنی عدم تشکیل پیوند اوربیتال دربردارنده ی آن نیست . در اینجا همان اتفاقی که در بنزن می افتد ، رخ خواهد داد . به این گونه که اوربیتال های 2pz اتم های مجاور همپوشانی کرده ، پیوند جانبی π (پای) تشکیل می دهند . از آنجایی که در هر لایه از گرافیت ، تعداد اتم های کربن بسیار زیاد است ، یک ابر الکترونی گسترده از این پیوند ها تشکیل می شود که الکترون های موجود در این ابر ، به راحتی می توانند در سرتاسر لایه حرکت کنند و جریان الکتریکی را انتقال دهند .
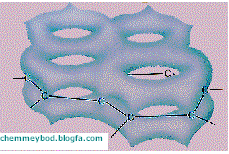
این موضوع را می توان بر اساس همپوشانی باند ظرفیت و باند رسانایی در گرافیت توصیف کرد
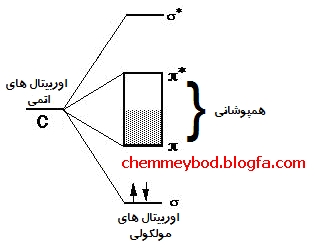
وجود جاذبه ی واندروالسی ( لوندون ) بین لایه های گرافیت را نیز می توان به پیدایش قطبیت های لحظه ای در این ابرها و القای آن به ابرهای مجاور نسبت داد .
 این وبلاگ توسط گروهی از دبیران و علاقه مندان به شیمی مدیریت می شود
این وبلاگ توسط گروهی از دبیران و علاقه مندان به شیمی مدیریت می شود